Segunda ley de la termodinámica
Probablemente la más conocida y de caso de estudio más profundo, ya que describe incluso los límites del universo, así como también nos advierte que el tiempo sigue una flecha de sola una dirección y que nuestro universo tiene un destino desolador y catastrófico.
La segunda ley de la termodinámica nos dice que: Cuando ocurre un proceso termodinámico, este ocurre en una sola dirección con respecto al tiempo, pero no viceversa.Es decir, que por ejemplo; si aventamos un vaso de cristal al suelo, este objeto "se romperá" y se dispersará en fragmentos sobre todo el piso, entonces aquí viene la pregunta. ¿Es posible qué de forma natural los fragmentos se reconstruyan nuevamente a la forma original que tenía antes el vaso?, es lógico que la respuesta sea NO, ya que se trata de un fenómeno irreversible, entonces aquí es donde viene el concepto y estudio de la segunda ley
Es imposible convertir completamente un tipo de energía a otro, sin que este cause pérdidas en el proceso.Esto es algo que en su momento podría parecer ilógico, pero si se analiza delicadamente podremos tener una respuesta más teórica y entendible del tema, en algunos casos nos toparemos con la definición de que, "la cantidad de entropía en el universo tiende a incrementarse con el tiempo".
Pero... ¿Qué es entropía? Pues bien, la entropía no es más que aquella cantidad de energía que no se puede aprovechar para producir un trabajo. Así también nos explica que se trata de un desorden total de las moléculas que esto complementa.
Por ejemplo; el universo constantemente se expande y por su desorden considerablemente va aumentando su entropía, hasta quedar sin energía necesaria para seguir transformándose, cuando ese momento llegue, todos los cuerpos alcanzarán un equilibrio térmico, de tal manera que sería el fin del universo entero.
curioso ¿no?
El estudio de las Máquinas Térmicas
A pesar de estas ideas y teorías que quizá un poco confusas para las personas que no eran científicos en ese tiempo, el avance de la termodinámica se formuló en un momento de gran optimismo tecnológico, con la llegada de la revolución industrial.
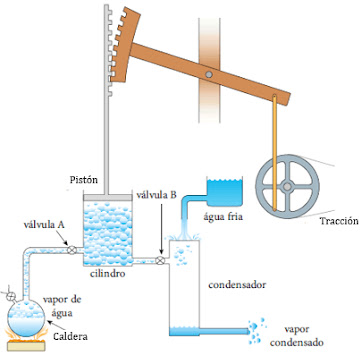
En la mitad del siglo 19, los físicos e ingenieros estaban construyendo máquinas de vapor para mecanizar el trabajo y el transporte y estaban tratando de encontrar la manera de hacerlos más potentes y eficientes. Grandes científicos como Clausius, Kelvin, Joule contribuyeron en gran medida, aunque en cierta parte se le considera como padre de esta disciplina al físico francés Sadi Carnot .Carnot demostró que se podía predecir la eficiencia máxima teórica de un motor de vapor mediante la medición de la diferencia de temperaturas del vapor en el interior del cilindro y la del aire que lo rodea, conocida en términos termodinámicos como los depósitos de agua caliente y fría de un sistema, respectivamente.
Formula de la segunda ley de la termodinámica
Q1: Calor Suministrado [Cal, Joules]
Resuelva los siguientes problemas.
1. ¿Cuál es la eficiencia de una máquina térmica a la cual se le suministrarán 9 000 calorías para obtener 20 200 Joules de calor de salida?
2.Calcular la eficiencia de una máquina térmica a la cual se le suministran 4.5. x 10^8 cal, realizando un trabajo de 5.3 x10^7 J.
3.¿Cuál es la eficiencia de una máquina térmica a la que se le suministran 8,350 calorías para obtener 23,860 J de calor de salida?
Tarea
Dibujar el ciclo de carnot, otto y el ciclo de Diesel.




.jpg)


Comentarios
Publicar un comentario